考前复习指导中考物理复习题
编辑:sx_liss
2014-05-28
【摘要】精品学习网为各位考生整理了考前复习指导中考物理复习题,希望可以帮考生一臂之力。
选择题
1. 理想气体模型的基本特征是
(A) 分子不断地作无规则运动、它们均匀分布在整个容器中
(B) 各种分子间的作用相等,各种分子的体积大小相等
(C) 所有分子都可看作一个质点, 并且它们具有相等的能量
(D) 分子间无作用力, 分子本身无体积
答案:D
2. 关于物质临界状态的下列描述中, 不正确的是
(A) 在临界状态, 液体和蒸气的密度相同, 液体与气体无区别
(B) 每种气体物质都有一组特定的临界参数
C)在以p、V为坐标的等温线上, 临界点对应的压力就是临界压力
(D) 临界温度越低的物质, 其气体越易液化
答案:D
3. 对于实际气体, 下面的陈述中正确的是
(A) 不是任何实际气体都能在一定条件下液化
(B) 处于相同对比状态的各种气体,不一定有相同的压缩因子
(C) 对于实际气体, 范德华方程应用最广, 并不是因为它比其它状态方程更精确
(D) 临界温度越高的实际气体越不易液化
答案:C
4. 理想气体状态方程pV=nRT表明了气体的p、V、T、n、这几个参数之间的定量关系,与气体种类无关。该方程实际上包括了三个气体定律,这三个气体定律是
(A) 波义尔定律、盖-吕萨克定律和分压定律
(B) 波义尔定律、阿伏加德罗定律和分体积定律
(C) 阿伏加德罗定律、盖-吕萨克定律和波义尔定律
(D) 分压定律、分体积定律和波义尔定律
答案:C
问答题
1. 什么在真实气体的恒温PV-P曲线中当温度足够低时会出现PV值先随P的增加而降低,然后随P的增加而上升,即图中T1线,当温度足够高时,PV值总随P的增加而增加,即图中T2线?
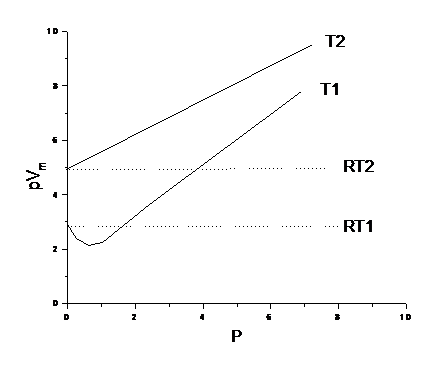
答:理想气体分子本身无体积,分子间无作用力。恒温时pV=RT,所以pV-p线为一直线。真实气体由于分子有体积且分子间有相互作用力,此两因素在不同条件下的影响大小不同时,其pV-p曲线就会出现极小值。真实气体分子间存在的吸引力使分子更靠近,因此在一定压力下比理想气体的体积要小,使得pVRT。
当温度足够低时,因同样压力下,气体体积较小,分子间距较近,分子间相互吸引力的影响较显著,而当压力较低时分子的不可压缩性起得作用较小。所以真实气体都会出现pV值先随p的增加而降低,当压力增至较高时,不可压缩性所起的作用显著增长,故pV值随压力增高而增大,最终使pV>RT。如图中曲线T1所示。
当温度足够高时,由于分子动能增加,同样压力下体积较大,分子间距也较大,分子间的引力大大减弱。而不可压缩性相对说来起主要作用。所以pV值总是大于RT。如图中曲线T2所示。
2.为什么温度升高时气体的粘度升高而液体的粘度下降?
答:根据分子运动理论,气体的定向运动可以看成是一层层的,分子本身无规则的热运动,会使分子在两层之间相互碰撞交换能量。温度升高时,分子热运动加剧,碰撞更频繁,气体粘度也就增加。但温度升高时,液体的粘度迅速下降,这是由于液体产生粘度的原因和气体完全不同,液体粘度的产生是由于分子间的作用力。温度升高,分子间的作用力减速弱,所以粘度下降。
3.压力对气体的粘度有影响吗?
答:压力增大时,分子间距减小,单位体积中分子数增加,但分子的平均自由程减小,两者抵消,因此压力增高,粘度不变。
4.两瓶不同种类的气体,其分子平均平动能相同,但气体的密度不同。问它们的温度是否相同?压力是否相同?为什么?
答:温度相同。因为气体的温度只取决于分子平移的动能,两种不同的气体若平移的动能相同则温度必然相同。但两种气体的压力是不同的,因为气体的压力与气体的密度是成正比的。两种气体的密度不同,当然它们的压力就不同。
【总结】精品学习网中考频道精心整理了考前复习指导中考物理复习题,可登录中考物理复习指导学习更多知识。
相关链接
标签:中考物理复习指导
免责声明
精品学习网(51edu.com)在建设过程中引用了互联网上的一些信息资源并对有明确来源的信息注明了出处,版权归原作者及原网站所有,如果您对本站信息资源版权的归属问题存有异议,请您致信qinquan#51edu.com(将#换成@),我们会立即做出答复并及时解决。如果您认为本站有侵犯您权益的行为,请通知我们,我们一定根据实际情况及时处理。